PROFESSIONNELS
INDICATIONS
du genou
de la hanche
de l’épaule
de la cheville
PROFESSIONNELS
du genou
de la hanche
de l’épaule
de la cheville
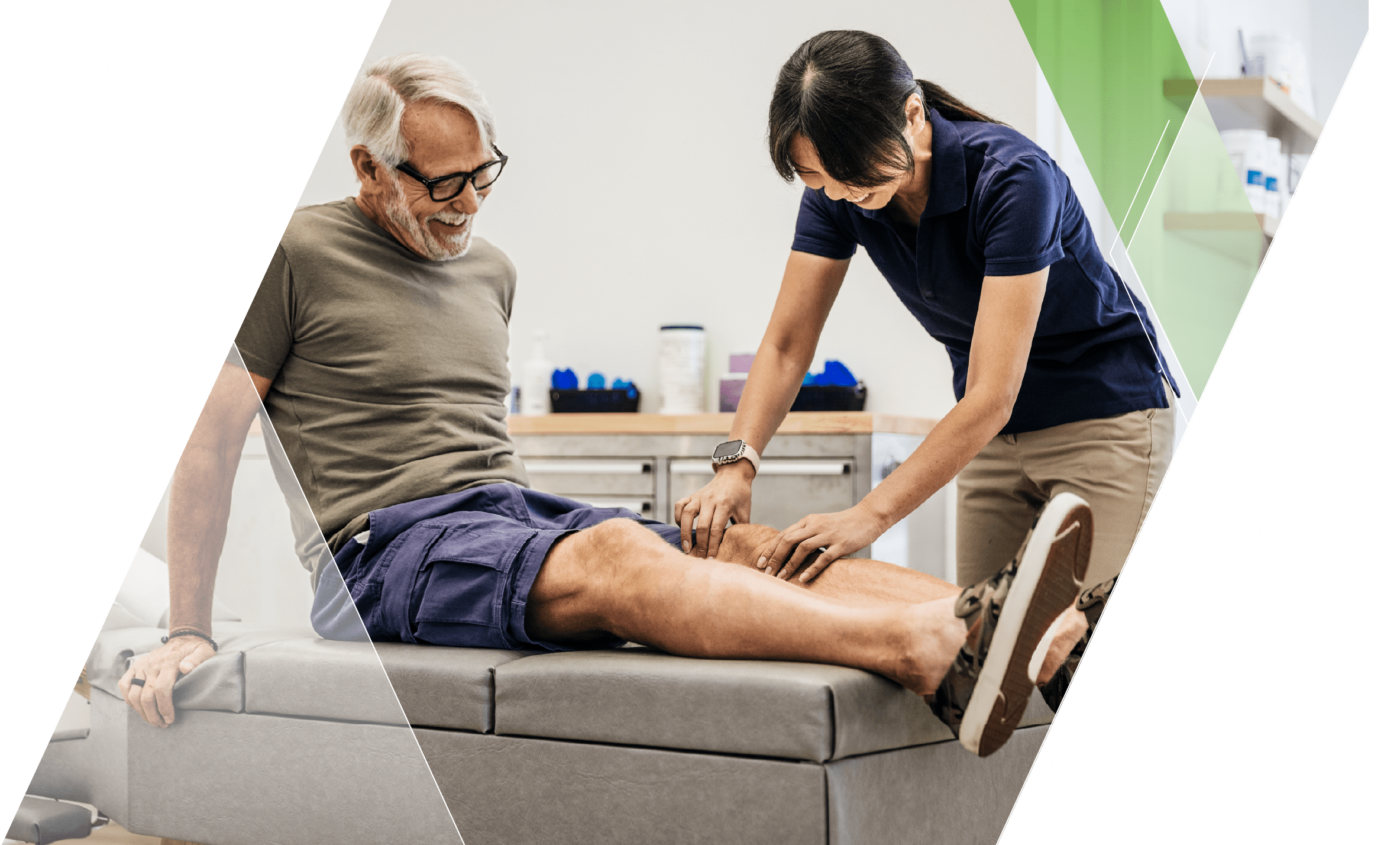
MonoviscMD est indiqué pour le traitement de la douleur causée par l’arthrose du genou, de la hanche, de l’épaule et de la cheville chez les patients qui n’ont pas répondu adéquatement au traitement conservateur non pharmacologique et aux analgésiques simples, ex. l’acétaminophène1.

La signification clinique comparative n’a pas été établie.

Réduction en pourcentage du score de douleur WOMAC dans le genou par rapport aux valeurs de départ avec CingalMD, MonoviscMD ou une solution saline, parmi la population en ITT**,††,‡‡,6,7


Mesures de l'innocuité
Cinq effets indésirables graves ont été signalés chez quatre sujets. Ces effets indésirables n’ont pas été considérés comme étant liés au traitement et ont disparu sans laisser de séquelles.
Les effets indésirables les plus fréquents étaient les céphalées, l’arthralgie, la douleur rachidienne, la dorsalgie et la rhinopharyngite. Six effets indésirables étaient liés au médicament à l’étude : l’arthralgie avec CingalMD (n = 2) et MonoviscMD (n = 2), un œdème périphérique avec CingalMD (n = 1) et une éruption cutanée avec MonoviscMD (n = 1).
Taux de répondeurs après 6 mois¶¶,3-5,7

Total d’AH par seringue; viscosuppléments en une injection unique

EXCELLENT PROFIL D’INNOCUITÉ POUR TOUTES LES INDICATIONS*,†,‡,§,3-5,7
Contre-indications :
Mises en garde et précautions pertinentes :
Pour de plus amples renseignements :
Veuillez consulter la notice d’emballage de MonoviscMD pour obtenir des renseignements importants au sujet des réactions indésirables et du mode d’emploi qui ne sont pas présentés dans ce document, ou visitez le www.monovisc.ca.
Vous pouvez également vous procurer la notice d’emballage en appelant au 1-888-550-6060 ou en écrivant à [email protected] .
Références :
1. Notice d’emballage de MonoviscMD. PENDOPHARM, mars 2025.
2. Petterson S, Plancher K. Single intra-articular injection of lightly cross-linked hyaluronic acid reduces knee pain in symptomatic knee osteoarthritis: a multicenter, double-blind, randomized, placebo-controlled trial.
Knee Surg Sports Traumatol Arthrosc.
2019;27(6):1992-2002.
3. Données internes. PENDOPHARM. Rapport d’étude clinique sur MonoviscMD
18-01.
4. Données internes. PENDOPHARM. Rapport d’étude clinique sur MonoviscMD
18-02.
5. Données internes. PENDOPHARM. Rapport d’étude clinique sur MonoviscMD
18-03.
6. Hangody L,
et al.
Intraarticular injection of a cross-linked sodium hyaluronate combined with triamcinolone hexacetonide (Cingal®) to provide symptomatic relief of osteoarthritis of the knee: a randomized, double-blind, placebo-controlled multicenter clinical trial.
Cartilage.
2018;9(3):276-283.
7. Données internes. Rapport d’étude clinique : Cingal 13-01.
8. Compendium des produits et spécialités pharmaceutiques. Monographie de Synvisc-One®. Genzyme Canada Inc., 2 mars 2009. Synvisc-One® est une marque déposée de Genzyme Corporation, É.-U.
9. Site Web de Durolane®. www.durolane.com, consulté le 13 janvier 2014. Durolane® est une marque déposée de Galderma S.A., Suisse.
10. Compendium électronique des produits et spécialités pharmaceutiques. Monographie de NeoVisc®. Tribute Pharmaceuticals Canada Inc. Consultée le 5 mars 2014. NeoVisc® est une marque déposée de Tribute Pharmaceuticals Canada Inc., Canada.
11. Baczkowicz D,
et al.
Effects of viscosupplementation on quality of knee joint arthrokinematic motion analyzed by vibroarthrography.
Cartilage.
2021;12(4):438-447.
12. Faivre J,
et al.
Crosslinking hyaluronic acid soft-tissue fillers: current status and perspectives from an industrial point of view.
Expert Rev Med Devices.
2021;18(12):1175-1187.